KI-unterstützte Bildbefundung
Eine an der Universität Basel entwickelte Machine-Learning-Software findet Einsatz in der klinischen Routine des
Universitätsspitals Basel.
Für die Neuroradiologie ist die Einführung der von künstlicher Intelligenz (KI) gestützten Software eine echte Innovation. Befundende Ärztinnen und Ärzte haben zukünftig die Möglichkeit, sich bei der Erkennung von Hirnläsionen unterstützen zu lassen. Der Algorithmus mit Namen MS-MD-GRU ist darauf trainiert, in Magnetresonanztomographie (MRI)-Aufnahmen des Gehirns von Patientinnen und Patienten mit Multipler Sklerose (MS) gesundes von krankem Gewebe zu unterscheiden und entsprechend geschädigte Hirnregionen zu markieren. Die Neuroradiologen überprüfen und korrigieren bei Bedarf die von der Software vormarkierten Bilder und verfassen auf dieser Basis wie gewohnt ihren Befund zuhanden der Neurologie.
Gut trainierter und verlässlicher Algorithmus
Gelernt hat MS-MD-GRU seine Aufgabe an rund 4000 MRI-Scans aus der in Basel geführten Swiss Multiple Sclerosis Cohort (SMSC). SMSC ist eine der grössten Datenbanken in Europa und USA für klinische Forschung zu MS. Sie enthält qualitativ hochwertige Daten von über 1600 Patientinnen und Patienten, darunter mehr als 7000 MRI-Untersuchungen des Gehirns. Prof. Dr. med. Cristina Granziera, Leitende Ärztin Neurologie und am Multiple Sklerose Center des Universitätsspitals Basel (USB), hat den Zugang zu SMSC koordiniert und als klinische Expertin an der Entwicklung von MS-MD-GRU mitgewirkt.
Ausführliche Tests dazu, wie verlässlich und genau MS-MD-GRU Hirnläsionen erkennt, haben gezeigt, dass die Übereinstimmung mit einer rein manuellen Befundung beinahe 80 Prozent beträgt. Dies ist ein im Vergleich zu kommerziell verfügbaren Produkten hoher Wert. Es ist möglich, so Dr. med. Johanna Lieb, stellvertretende Leiterin Neuroradiologie, dass die Analyse von MRI-Untersuchungen durch den Algorithmus akkurater und stabiler wird als sie jetzt ist, wenn die Aufnahmen nur vom menschlichen Auge allein bewertet werden. Johanna Lieb kennt die Fähigkeiten von MS-MD-GRU. Auch sie war klinische Expertin in diesem Projekt.
Aus der Forschung in die klinische Praxis
Der Algorithmus wurde initial von Prof. Philippe Cattin, PhD MSc, Leiter des Department of Biomedical Engineering (DBE), und seinem ehemaligen Doktoranden Simon Andermatt entwickelt. Als Software, die Hirnstrukturen auf MRI-Bildern automatisiert erkennen und markieren kann, wurde MD-GRU, wie der Algorithmus hiess, als sie noch nicht spezifisch auf MS-Hirnläsionen trainiert war, mehrfach erfolgreich in Forschungsprojekten eingesetzt.

«Es ist schön zu sehen, wie unsere langjährige Forschungsarbeit den Patientinnen und Patienten in Basel zugutekommt.»
Prof. Philippe C. Cattin, PhD, MSc
Leiter Department of Biomedical Engineering
Eine klinische Anwendung von MD-GRU war ein erklärtes Ziel von Philippe Cattin. Die gangbare Lösung bot sich über eine gesetzliche Sonderregelung für akademische Eigenentwicklungen. Software zur Unterstützung von Diagnose- und Therapieentscheidungen wird nämlich grundsätzlich als Medizinprodukt definiert und unterliegt den entsprechenden, teilweise aufwändigen Regulierungen. So bestimmt es die Europäische Medical Device Regulation (MDR), auf die sich auch die Schweizer Gesetzgebung stützt. Entwicklungen, die innerhalb einer akademischen Gesundheitsorganisation entstehen und nur dort genutzt werden, können laut MDR allerdings unter vereinfachten Bedingungen für die Nutzung im klinischen Alltag zugelassen werden. Beides, akademische Eigenentwicklung und «in house»-Nutzung, treffen auf MS-MD-GRU zu.
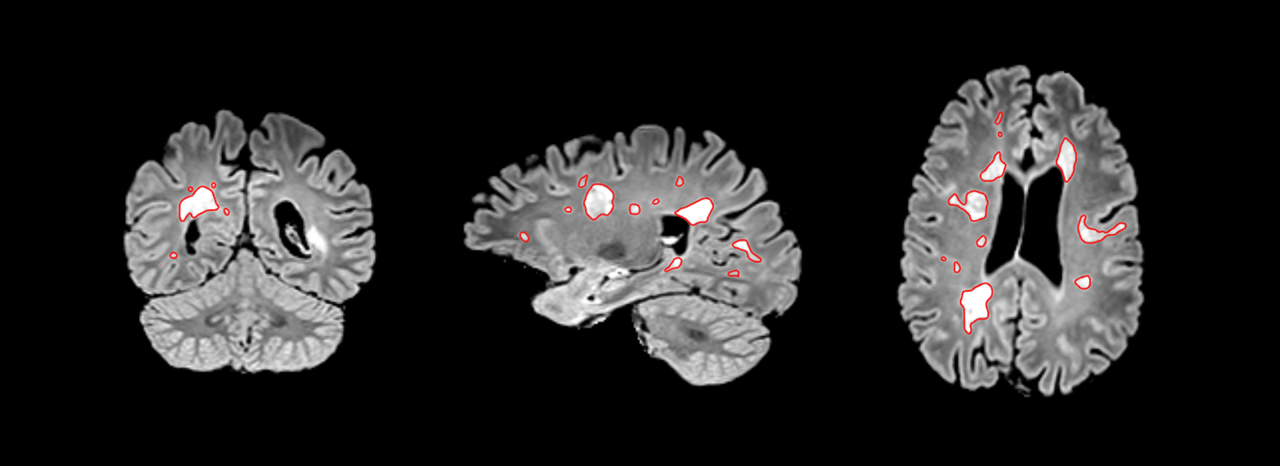
MS-MD-GRU basiert auf einer Machine-Learning-Software, die Hirnläsionen auf MRI-Bildern von Patientinnen und Patienten mit Multipler Sklerose erkennt und direkt auf dem Scan markiert. Im Rahmen der üblichen Befundung werden die von der KI identifizierten Segmentierungen durch eine Neuroradiologin bzw. einen Neuroradiologen überprüft und allenfalls korrigiert.

«Die Integration dieser KI in die bestehenden klinischen Prozesse ist hoch innovativ. Oft fehlt der Industrie das Verständnis dafür, was die Radiologie wirklich benötigt. Wir als internes Forschungsteam sind der ideale Partner, um diese Lücken zu schliessen.»
Shan Yang, PhD
Wissenschaftlicher Mitarbeiter Forschungskoordination, Radiologie und Nuklearmedizin, Universitätsspital Basel
Am Departement Klinische Forschung (DKF) fand Philippe Cattin schliesslich die nötige Expertise in den Bereichen Regulatorik, Qualitätsmanagement und Systemvalidierung. Gemeinsam mit Roland John, Leiter Quality Affairs am DKF, und mit Unterstützung von Dr. Bram Stieltjes, Leiter Forschungskoordination im Bereich D & ICT am USB, wurde so das Projekt vorangetrieben. Roland John hat gemeinsam mit Kollegin Claudia Saupper, Senior IT-Spezialistin, das ISO 13485-konforme Qualitätsmanagement aufgebaut und die behördlich nötige technische Dokumentation geführt. Als unabhängige Gutachter wurden Experten der auf Medizinprodukte spezialisierten Firma Effectum Medical AG hinzugeholt.
Integration in die Klinikprozesse
An KI-Anwendungen für automatisierte Bilderkennung wird eigentlich schon lange geforscht. Auch liegen vielversprechende Ergebnisse vor. Dennoch werden sie in der Radiologie bislang kaum genützt, sagt Shan Yang, PhD, wissenschaftlicher Mitarbeiter Forschungskoordination an der Radiologie und Nuklearmedizin am USB. Das Hauptproblem, führt er aus, liegt an der mangelnden Integration in die bestehenden Abläufe. Dies führe dazu, dass kommerzielle KI-Systeme zwar Bilderkennung durchführen und Markierungen setzen können, diese aber nicht editierbar sind. Sie müssten manuell übertragen werden, was zu Fehlern führen kann und den Arbeitsaufwand eher erhöht als Effizienz schafft.
Die Aufgabe von Shan Yang ist es, MS-MD-GRU so in die bestehenden klinischen Abläufe einzubetten, dass die Radiologinnen und Radiologen die KI-generierten Markierungen als zusätzliche Ebene direkt auf den Bildern angezeigt bekommen und diese bei Bedarf korrigieren können. Die finalen Ergebnisse werden zusammengefasst und direkt dem radiologischen Befund hinzugefügt. Auch Verlaufskontrollen werden so deutlich einfacher und effizienter. Dies wiederum kann die Behandlungsqualität vor allem bei chronischen Erkrankungen wie MS deutlich verbessern.
Erst der Anfang
MS-MD-GRU hat grosses Potenzial für weitere Anwendungen und stellt erst den Anfang der KI-gestützten Diagnosestellung und Therapieentwicklung dar. Laut Johanna Lieb ist es beispielsweise denkbar, dass der Algorithmus über seine Anwendung bei MS hinaus für die Evaluation sämtlicher Erkrankungen der weissen Hirnsubstanz weiterentwickelt werden kann. Auch weitere Schritte in Richtung automatisierter Befundung oder Befundvergleiche wären möglich.
Besonders erfreulich an diesem Projekt ist die erfolgreiche interdisziplinäre und interinstitutionelle Kollaboration, der diese Innovation zu verdanken ist. Es hat Vorzeigecharakter, wenn zwei universitäre Departemente – DBE und DKF – gemeinsam mit drei klinischen Abteilungen – Neuroradiologie, Neurologie und Bereich D & ICT – die klinische Praxis auf höchstem technischem Niveau voranbringen. Rein akademisch und durch Stiftungsgelder finanziert.
«Mit dem Pilotprojekt MS-MD-GRU haben wir gezeigt, dass wir Forschungsergebnisse in den klinischen Prozess integrieren können und dabei die regulatorischen Anforderungen erfüllen.»
Roland John
Leiter Quality Affairs, Departement Klinische Forschung

MS-MD-GRU-Projektteam
Projektidee
- Prof. Philippe C. Cattin, Leiter DBE
- Dr. Bram Stieltjes, PhD, Leiter Forschungskoordination, Bereich D&ICT, USB
- Prof. Oliver Bieri, Leiter Radiologische Physik, Radiologie und Nuklearmedizin, USB
Projektkoordination
- Prof. Philippe C. Cattin, Leiter DBE
- Roland John, Leiter Quality Affairs, DKF
Klinische Expertinnen
- Dr. Johanna Lieb, Stv. Leitung Neuroradiologie, USB
- Prof. Cristina Granziera, Leitende Ärztin Neurologie, Multiple Sklerose Zentrum, USB
Algorithmus- und Software-Entwicklung
- Dr. Simon Andermatt, IT-Entwickler, DBE
- Vitor Gouveia, Software-Entwickler, DBE
- Stefan Weber, Software-Entwickler, DBE
Qualitätsmanagement und technische Dokumentation
- Roland John, Leiter Quality Affairs, DKF
- Claudia Saupper, Senior IT-Projektleiterin, DKF
Regulatorik
- Claudia Becherer, Teamleiterin Regulatorik, DKF
DKF Integration in klinische Routine
- Shan Yang, PhD, Wissenschaftlicher Mitarbeiter, Radiologie und Nuklearmedizin, USB
Unabhängige Gutachter
- Prof. Marco Düring, Co-CEO und CSO, MIAC AG
- Rolf Kaufmann, PhD, Senior Medical Device Expert, Effectum Medical AG
- Georg Lambert, PhD, Clinical Evaluation, Effectum Medical AG
Funding
Stiftung zur Förderung der gastroenterologischen und allgemeinen klinischen Forschung sowie der medizinischen Bildauswertung, Basel
November 2024
© Departement Klinische Forschung, Universität Basel c/o Universitätsspital Basel, November 2024